Rilascio controllato di farmaci da biomateriali
Responsabili: Anna Tampieri, Monica Sandri, Simone Sprio, Michele Iafisco
Personale coinvolto: Elisabetta Campodoni, Massimiliano Dapporto, Francesca Carella, Marta Tavoni, Lorenzo Degli Esposti
Le patologie del tessuto osseo possono avere cause traumatiche o metaboliche. Queste ultime si riferiscono ad alterazioni del fisiologico metabolismo dell’osso, innescate da infezioni e infiammazioni (es. osteomieliti) o processi neoplastici (es. osteosarcomi).
La chirurgia ortopedica necessita frequentemente di accessi invasivi per il trattamento di molte patologie, elevando il rischio di infezioni da microrganismi patogeni (es. batteri) soprattutto in ambiente ospedaliero. In particolare, i patogeni possono colonizzare sia il campo operatorio che la superficie dei biomateriali impiantati, compromettendo l’esito della chirurgia.
Per questo motivo, si ricorre spesso alla somministrazione di antibiotici come trattamenti pre-, peri- e post-operatori mirati alla riduzione del rischio di infezione.
Negli ultimi anni la Ricerca Scientifica sta cercando di rispondere ad una crescente richiesta di soluzioni impiantabili che possano veicolare farmaci in situ, ovvero veicolati all’impianto stesso, eliminando quindi gli effetti indesiderati derivati da elevate somministrazioni sistemiche.
I biomateriali sviluppati in ISSMC-CNR nell’ambito della rigenerazione ossea, sono caratterizzati da elevata biocompatibilità e biomimetismo, ovvero riproducono fedelmente le caratteristiche chimico-fisiche, morfologiche e meccaniche del tessuto osseo, e si pongono inoltre come ottimi candidati per la ricerca di sistemi di rilascio controllato di farmaci in situ.
Gli approcci per realizzare il caricamento (loading) del farmaco in un dispositivo sono molteplici, dall’introduzione di componenti che contengono il farmaco, all’adsorbimento superficiale mediante immersione in soluzioni farmaceutiche.
Per tali studi di caricamento e rilascio di farmaco, sono stati scelti alcuni biomateriali sviluppati in ISSMC-CNR:
- cementi ossei, ovvero miscele autoindurenti iniettabili in chirurgia mininvasiva;
- scaffolds macroporosi ottenuti da tecniche di formatura quali replica o foaming diretto;
- scaffolds ibridi costituiti da fibre di collagene di tipo I auto-assemblate e mineralizzate con nano particelle di idrossiapatite contenente ioni Magnesio
I farmaci selezionati per gli studi di rilascio controllato includono antibiotici, in particolare Vancomicina (antibiotico comunemente utilizzato nel trattamento delle infezioni da batteri Gram+, come Staphylococcus Aureus, responsabile dell’osteomielite) e Gentamicina, un inibitore di sintesi proteica a più ampio spettro ed anche farmaci sperimentali specifici per sconfiggere le osteomieliti.
Altri farmaci in fase di studio includono antitumorali per il trattamento di patologie neoplastiche come l’osteosarcoma. A seguito dell’asportazione chirurgica della massa tumorale, le due principali criticità da fronteggiare sono la ricreazione di tessuto osseo in lacune anche di grandi dimensioni, da una parte, e la difficile totale eradicazione delle cellule neoplastiche, dall’altra. In questo caso, un biomateriale impiantato per colmare la lacuna ossea, in assenza di ulteriori accorgimenti farmacologici non potrebbe escludere la formazione di recidive tumorali. In questo contesto, la possibilità di rilasciare farmaci antitumorali da biomateriali può risultare strategico verso la completa rigenerazione ossea post-chirurgica. I farmaci antitumorali selezionati per questi studi includono doxorobucina, metotrexato o molecole più specifiche per target therapy quali anticorpi anti-RANKL e anti-mTOR.
Gli incoraggianti risultati ottenuti da queste ricerche aprono nuove prospettive per lo sviluppo di biomateriali medicati.
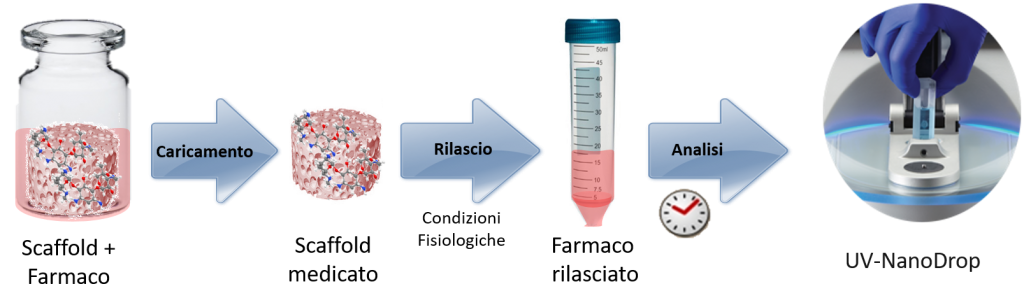
Strumenti e Processi
Il caricamento del farmaco sul biomateriale può avvenire con molteplici strategie, tra cui l’adsorbimento superficiale mediante immersione in soluzione medicata o l’introduzione nel biomateriale di nanoparticelle o microcapsule polimeriche o ibride precedentemente funzionalizzate con i farmaco.
La struttura chimica dei farmaci è molto rilevante nella scelta della tecniche analitiche adatte alla quantificazione cinetica, nel tempo, del rilascio. Tra queste, si cita la spettroscopia UV visibile (NanoDrop™ OneC Microvolume UV-Vis Spectrophotometer).
In ISSMC-CNR, gli studi di rilascio di farmaco vengono condotti in mezzi liquidi tali da replicare la composizione fisiologica dei fluidi del corpo umano.
Principali collaborazioni
- Finceramica
- Greenbone
- IRST
- IOR
- IRET
Progetti
- BIOBOS
- DINAMICA